服務熱線
15150888188
問題6:飲用水與自來水,是一回事嗎?
自來水與飲用水是兩個不一樣的術語與概念。
自來水:是指通過自來水處理廠凈化、消毒后生產出來的符合相應標準的供人們生活、生產使用的水。生活用水主要通過水廠的取水泵站汲取江河湖泊及地下水,地表水,由自來水廠按照《國家生活飲用水相關衛生標準》,經過沉淀、消毒、過濾等工藝流程的處理,最后通過配水泵站輸送到各個用戶。自來水在中國大陸一般不被用來直接飲用,但在世界某些地區由于采用了較高的質量管理標準而直接飲用。
飲用水:是指供人生活的飲水和生活用水。飲用水包括干凈的天然泉水、井水、河水和湖水,也包括經過處理的礦泉水、純凈水等。加工過的飲用水有瓶裝水、桶裝水、管道直飲水等形式。2007年7月1日,衛生部和國家標準化管理委員會聯合發布新的《生活飲用水衛生標準》(GB 5749-2006),該標準具有三個特點:加強了對水質有機物、微生物和水質消毒等方面的要求,該標準中的飲用水水質指標由原標準(GB 5749-85)的35項增至106項;統一了城鎮和農村飲用水衛生標準;參考了世界衛生組織的《飲用水水質準則》,實現飲用水標準與國際接軌。由于中國地域廣闊,各地具體情況不同,新標準中的水質全部指標最遲于2010年7月1日實施。中國《藥品生產質量管理規范》(2010版)第99條規定:藥品生產用水應適合其用途,應至少采用飲用水作為制藥用水原料水。
自來水與飲用水是兩個概念。制藥行業中,最低級別的制藥用水為飲用水,基于國情考慮,大多數企業只能采用自來水為制藥用水的原水。如果自來水水質不符合飲用水標準,制藥企業需將自來水引入制水間進行凈化處理,遵照中國GMP規定,自來水不允許直接用于制藥生產環節(包括洗手、潔具清洗)。原則上來講,飲用水工程為國家工程,自來水企業有責任輸送符合國家標準的飲用水到各個制藥企業的制水間,飲用水水質判斷標準不能僅限于自來水企業的設備出口,應該延伸到各個用水點用戶處。
這個責任誤區主要是市政管網無法時刻輸送給企業符合GB的飲用水,導致企業需要自行進行凈化處理,在自行凈化自來水的過程中,產生了一系列將預處理列入純化水機的“中國特色”的誤區。
問題7:以飲用水為水源,經過蒸餾法制備的注射用水內毒素水平在什么級別?
注射用水的內毒素藥典標準為不高于0.25EU/ml,飲用水中的內毒素含量水平大概在10-100EU/ml水平,飲用水經純化水機凈化后,其內毒素水平大概會在1-10EU/ml水平,相當于傳統預處理+RO/EDI的純化水機的內毒素去除能力為1-2log水平。蒸餾法分為三種:單效蒸餾、多效蒸餾與熱壓蒸餾,目前,單效蒸餾水機因不節能等原因,已被淘汰。工業化生產的制藥企業普遍采用的是多效蒸餾水機與熱壓蒸餾水機。揚州亞飛主要生產的是多效蒸餾水機,采用降膜式外加三級分離技術,是目前國內制藥行業的首選。
通常情況下,熱壓蒸餾水機的內毒素去除能力大概在2-3log水平,也就是說,采用飲用水直接制備注射用水時具有一定的風險性,但采用純化水經熱壓蒸餾水機制備注射用水時,內毒素含量低于0.1EU/ml,中國藥典規定:注射用水需采用純化水經蒸餾制備而得,因此,企業采用熱壓式蒸餾水機在中國制藥企業使用是完全安全的。
多效蒸餾水機因設計不同,內毒素去除能力不盡相同,例如,采用升膜法設計的多效蒸餾水機,內毒素去除能力大概在2-3log水平;采用降膜法+外螺旋分離設計的多效蒸餾水機,內毒素去除能力最高可以達到3-4log水平。美國藥典允許注射用水采用飲用水經蒸餾制備而得,主要是基于部分多效蒸餾水機具有3-4log的內毒素去除能力,飲用水為原水時,也能得到內毒素含量低于0.01EU/ml的注射用水。
揚州亞飛主要生產的是多效蒸餾水機,采用降膜式外加三級分離技術,是目前國內制藥行業的首選。
問題8:純蒸汽與工藝蒸汽的區別是什么?
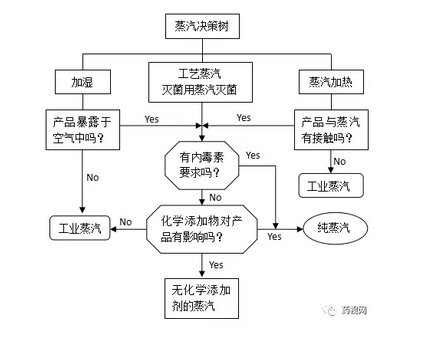
蒸汽在制藥企業中是一種重要的公共工程,主要為制藥用水的制備、工藝設備的溫度控制提供熱源,用于無菌工藝設備、器具、最終滅菌產品的滅菌等。蒸汽可大致分為工業蒸汽(Plant Steam或Black Steam)、工藝蒸汽(Process Steam)和純蒸汽(Pure Steam或Clean Steam)。
工業蒸汽主要用于非直接接觸產品的加熱,為非直接影響系統,又可細分為普通工業蒸汽和無化學添加蒸汽。普通工業蒸汽是指由市政用水軟化后制備的蒸汽,屬于非直接影響系統,用于非直接接觸產品工藝的加熱,一般只要考慮系統如何防止腐蝕;無化學添加蒸汽是指由純化過的市政用水添加絮凝劑后制備的蒸汽,屬于非直接影響系統,主要用于空氣加濕,非直接接觸產品的加熱,非直接接觸產品工藝設備的滅菌,廢料廢液的滅活等。無化學添加蒸汽中不應該含有氨、肼等揮發性化合物。
工藝蒸汽屬于直接影響系統,主要用于最終滅菌產品的加熱和滅菌,冷凝液最少應該滿足城市飲用水的標準。
純蒸汽屬于直接影響系統,經蒸餾方法制備而成,冷凝液需滿足注射用水的要求。純蒸汽用于濕熱滅菌工藝時,還需在不凝性氣體、過熱度和干燥度方面達到EN285和HTM2010等標準的要求。純蒸汽是由原水制備,所使用的原水是經過處理并至少滿足飲用水要求,不少企業會采用純化水或注射用水制備純蒸汽,純蒸汽不含揮發性添加劑,因此不會受到胺類或肼類雜質的污染,這對于預防注射劑產品的污染是極其重要的。
在蒸汽系統設計過程中采用哪種質量標準的蒸汽,可參考ISPE推薦的決策樹,如下圖所示。
問題9:采用飲用水為源水,通過傳統預處理+RO/EDI的純化水機工藝,純化水內毒素水平在什么級別?
注射用水的內毒素藥典標準為不高于0.25EU/ml,飲用水中的內毒素含量水平大概在10-100EU/ml水平,飲用水經純化水機凈化后,其內毒素水平大概會在0.1-1EU/ml水平,相當于傳統預處理+RO/EDI的純化水機的內毒素去除能力為2-3log水平。實際上,國外有些企業,直接用飲用水+預處理+RO/EDI實現注射用水的制備。
問題10:腸道吸收與非腸道吸收對于制藥用水的本質區別是什么?
腸道吸收藥物因為通過了腸道的“過濾”作用,對制藥用水中的內毒素指標沒有要求;非腸道吸收藥物,例如注射劑,因為沒有經過腸道“過濾”,對制藥用水中的內毒素指標往往具有很高的要求,否則容易引起熱原反應。這也是純化水與注射用水水質指標中一個非常明顯的差異。需要注意的是:腸道吸收時,不允許有大腸桿菌的污染,這也是飲用水指標中明確“大腸桿菌不可見”的主要原因。
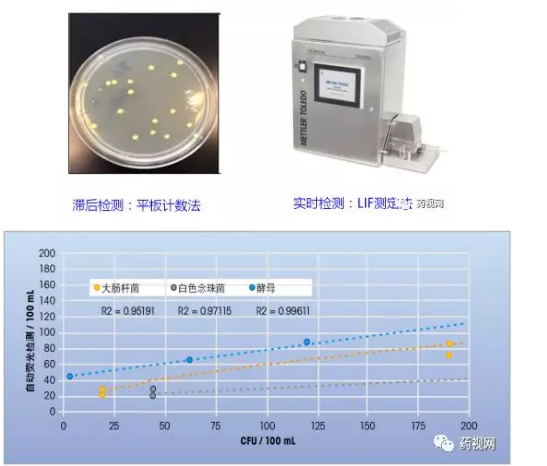
問題11:在線微生物限度檢測儀器對傳統平板計數法帶來了哪些革命性的沖擊?
與TOC檢測法顛覆易氧化物檢測法類似,“激光誘導熒光光譜(LIF)測量技術”顛覆了“平板計數法”,它科學地解決了“大多數微生物是無法培養成菌落數的”這一客觀存在的現實問題,因此,在線微生物檢測技術將很可能帶來世界范圍內微生物限度檢測標準的重新制定。
建立以“激光誘導熒光光譜(LIF)測量技術”為背景的微生物限度標準及PQ執行措施,是一個全新的課題。它將不僅是對中國制藥行業的挑戰,也是對包括美國在內的全世界范圍內制藥用水微生物檢測技術與標準的挑戰。
與在線TOC檢測技術類似,激光誘導熒光光譜(LIF)測量的實時微生物檢測技術將在接下來的10年會直接推動具有微生物檢測需求的的行業,例如半導體或電子行業,但制藥行業因為對微生物的檢測實時性需求并不是最緊迫需求,制藥用水藥典指標檢測方法的更新相對較慢,但相信未來還是會帶來很大的變革的,比較PAT技術是主導發展方向。